问题详情
图为一带可移动隔板的密闭容器,某温度下,左、右两侧反应均达平衡,此时隔板处于容器中央。若保持温度不变,向左侧容器中充入一定量的H2,下列说法正确的是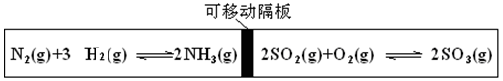
A.两侧平衡均向正反应方向移动
B.左侧平衡向逆反应方向移动
C.右侧平衡向逆反应方向移动
D.两侧平衡均向逆反应方向移动
相关标签: 逆反应
未找到的试题在搜索页框底部可快速提交,在会员中心"提交的题"查看可解决状态。
收藏该题
查看答案
相关问题推荐
-
下列情况一定能说明化学反应处于平衡状态的是
A.正反应速率与逆反应速率相等
B.正反应和逆反应同时进行
C.反应物与生成物共存
D.反应物和生成物的总质量保持不变
-
可逆反应达到平衡的主要特征是()
A.反应停止了
B.正、逆反应的速率均为零
C.正、逆反应都还在进行
D.正、逆反应的速率相等
-
下列叙述正确的为( )。
A、化学平衡状态是正、逆反应都停止的状态
B、反应
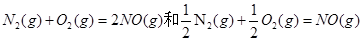 代表同一反应,所以标准平衡常数相等
代表同一反应,所以标准平衡常数相等C、反应
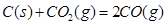 的
的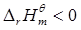 ,一定温度下达到平衡后,降低压力,正、逆反应速率都减慢,但平衡向右移动
,一定温度下达到平衡后,降低压力,正、逆反应速率都减慢,但平衡向右移动D、多步反应的总平衡常数为各步反应平衡常数之和
-
对于可逆反应2A(气)+B(气)
 2C(气) △H﹤0正确的说法是
2C(气) △H﹤0正确的说法是A.增加A的浓度,平衡向右移动,K值增大
B.增加压强,正反应速度增大,逆反应速度减小,平衡向右移动
C.使用正催化剂,化学平衡向右移动
D.降低温度,正逆反应速度都减慢,化学平衡向右移动
-
下列叙述中不正确的是?
A.增加反应物的浓度可使正反应速率增加B.反应温度升高可同时加快正、逆反应速率C.提高反应物的浓度,可降低活化能D.加入催化剂,可降低正、逆反应的活化能,提高反应速率
